技术溯源 · STED Microscopy
重写光学边界的
一百年方程
1873年,物理学家 Ernst Abbe 以一个简洁的方程为光学显微镜划定了边界:分辨率极限约为200nm,半个光波长。这道"铁律"统治科学界逾百年,被认为是不可逾越的物理约束。直到1994年,德国科学家 Stefan W. Hell 提出 STED 技术原理——以一束甜甜圈形的耗尽光抹去激发光斑的外缘,将发光区域压缩至衍射极限以下。从理论到实验,他用了六年时间颠覆了阿贝定律。此后,PALM、STORM 等超分辨技术相继兴起,2014年,这场"分辨率革命"最终以诺贝尔化学奖落幕。
三束光改写分辨率
STED 的核心思想并非"看得更精准",而是"让不该发光的分子闭嘴"——这是一种对荧光分子的主动控制
激发束聚焦
第一束脉冲激光被高 NA 物镜聚焦为衍射极限尺寸的光斑(约200nm),将目标区域内的荧光分子从基态激发至激发态,准备发出荧光
Excitation Pulse甜甜圈形耗尽光
紧随其后的第二束耗尽光(STED beam)被整形为中心零强度的环形分布。它强制外围的激发态分子发生受激发射而淬灭,使其无法自发发光,只有中心微小区域的分子得以保留激发态。
STED Depletion Beam纳米级发光点重建图像
幸存发光区域的等效点扩展函数(PSF)远小于衍射极限,可降至40nm甚至更低。通过逐点扫描,系统以纳米精度重建出完整的超分辨荧光图像。
Sub-diffraction PSF从枷锁到诺贝尔奖
超分辨荧光显微技术的诞生,是几代科学家前赴后继挑战物理定论的故事

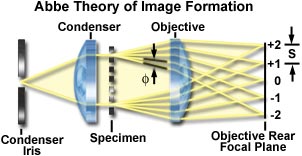
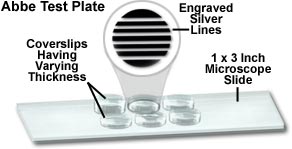
阿贝衍射极限
物理学家 Ernst Abbe 推导出著名的分辨率极限公式 d = λ/2NA,确立可见光显微镜的理论分辨上界约 200nm。这一定律被物理学界奉为铁律,此后统治光学成像领域超过百年。

Optics Letters, 1994 · Hell & Wichmann
STED 理论横空出世
Stefan W. Hell 与 Jan Wichmann 在《光学快报》(Optics Letters)发表开创性论文,首次提出通过受激发射损耗(Stimulated Emission Depletion)突破衍射极限的理论框架。这一设想在当时被众多物理学家视为异想天开,Hell 四处奔走却难以获得资助。
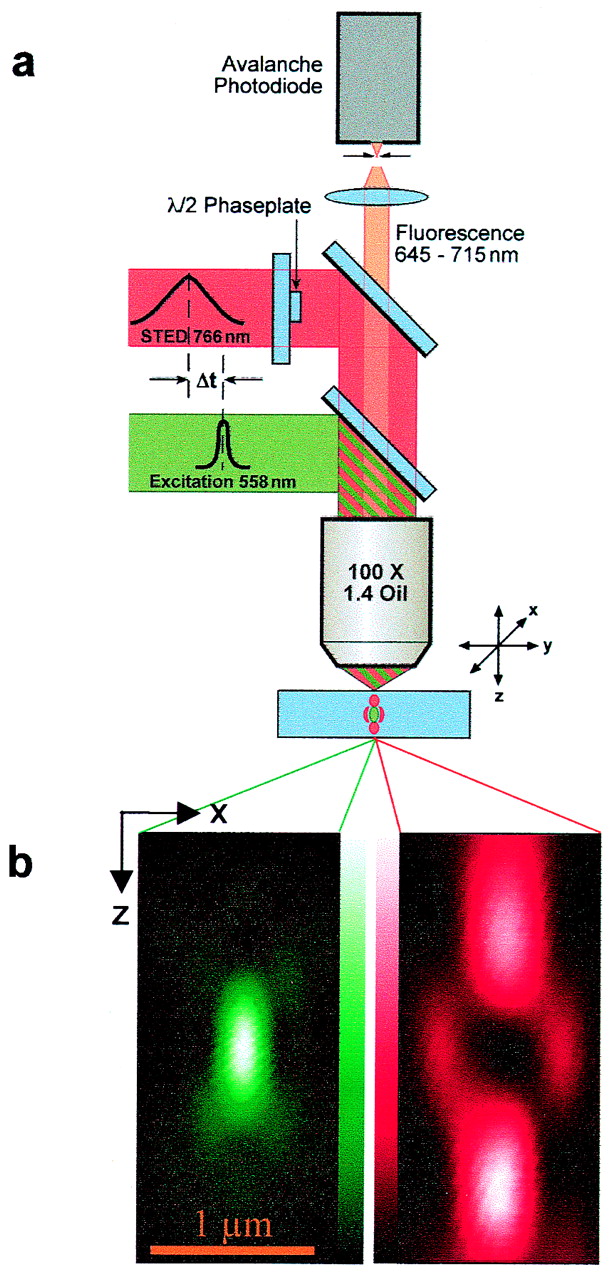
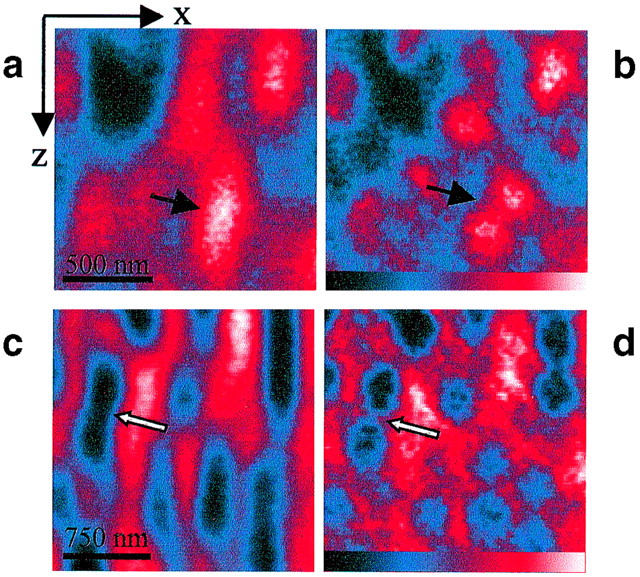
首次突破:100nm 分辨率
经过六年的实验攻坚,Hell 团队在马克斯·普朗克生物物理化学研究所成功搭建出第一台 STED 显微镜,实现约 100nm 的空间分辨率,成果发表于《美国国家科学院院刊》(PNAS)。衍射极限这道"铁律"被正式打破,超分辨显微成像的时代由此开启。

结构光照明:另辟蹊径
Mats Gustafsson 提出饱和结构光照明显微技术(SSIM),利用非线性荧光响应与空间频率移位实现超分辨成像,分辨率突破衍射极限的五分之一,为超分辨技术提供了全新路线。SSIM 不依赖单点扫描,更适合宽视野快速成像场景。
-%20Developing%20PALM%20Microscopy.jpg)
PALM 与 STORM 双剑合璧
Eric Betzig 与 Harald Hess 创立光激活定位显微技术(PALM),通过稀疏激活单分子荧光并精确定位中心坐标来重建超分辨图像
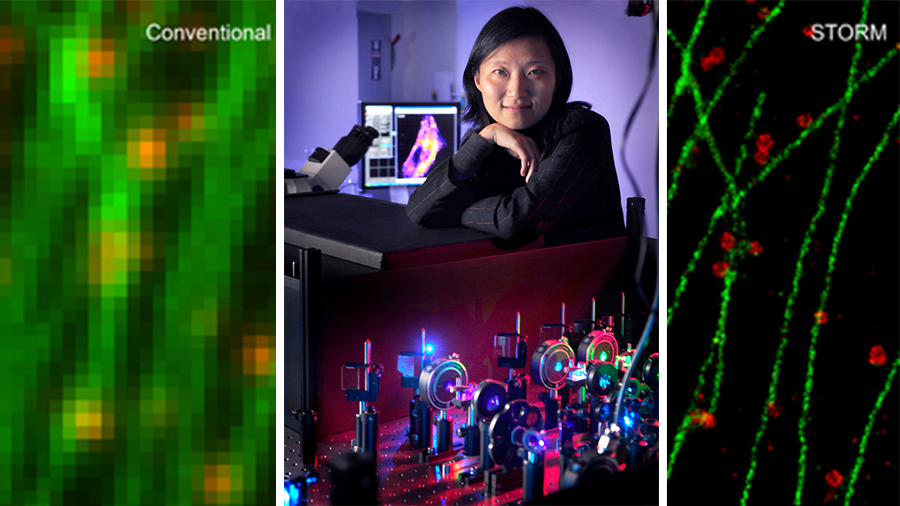
同年,哈佛大学庄小威团队发明随机光学重构显微技术(STORM),采用可切换荧光探针实现类似突破。两种基于单分子定位的技术路线与 STED 殊途同归,推动超分辨成像进入多元格局。

诺贝尔化学奖:分辨率革命的终章
瑞典皇家科学院将诺贝尔化学奖授予 Stefan W. Hell、Eric Betzig 与 William E. Moerner,表彰三人在超分辨荧光显微技术领域的革命性贡献。颁奖词写道:"他们的工作将光学显微镜带入了纳米维度,使人类得以在活体细胞中追踪单个分子的运动。" STED、PALM、STORM 三条技术路线共同构成了这场历时二十年的"分辨率革命"。
STED 改变了哪些研究领域
超越衍射极限的分辨率,使 STED 显微技术在多个前沿学科中成为不可替代的观测手段
神经生物学
突触间隙仅约20nm,远低于衍射极限,STED 可在活体组织深层直接分辨突触小泡、PSD蛋白复合体及树突棘的纳米形态,揭示神经可塑性机制。配合深层组织成像模块,支持活鼠脑内长时程动态追踪。
细胞生物学
线粒体嵴、内质网网络、核孔复合体等亚细胞结构尺寸普遍在50–200nm范围,共聚焦分辨率远不足以区分。STED 实现真实形态的直接观测,无需电子显微镜制样即可在活细胞中捕获动态重组过程。
膜生物学
细胞膜上的脂质筏、受体聚集与扩散是高度动态的纳米事件。STED 与荧光探针结合,可在活细胞上实时追踪单个膜蛋白的横向运动与相分离,为信号转导研究提供直接证据。
微生物学
解析原核生物及真菌的亚细胞结构,研究宿主-病原体相互作用界面
活细胞成像
专用低光毒性染料与模块,在最小损伤下记录细胞器动态与分裂过程
病毒学
实时捕获病毒颗粒侵入、衣壳解组装及出芽成熟的纳米尺度动态过程
生物物理学
在纳米尺度测量蛋白质相互作用力、扩散系数与分子马达的运动步长
植物科学
从完整植株到蛋白质复合体,跨尺度成像细胞壁、叶绿体与气孔动态
生理学
跨多尺度研究心肌细胞、肾小管及腺体在生理刺激下的实时功能响应
材料科学
利用超分辨荧光标记观测固态材料中的缺陷分布、扩散与相变动力学
动物学
克服自发荧光与组织深度限制,解析模式生物各发育阶段的精细结构
核心专利与 Stable-STED 技术
瑞霏仪器依托中科院核心成果,将实验室级 STED 技术转化为高稳定性商业系统,并在工程化层面实现多项突破
Stable-STED 全光纤模块
全光纤激光耦合设计,从根本上解决了传统 STED 需每日手动校准光路的难题,纳米级光斑长期漂移极小,实验连续性大幅提升
一键式超分辨重构算法
基于硬件参数感知的自适应重构算法,无需复杂调参即可获取高保真超分辨图像,将 STED 成像门槛降至普通共聚焦系统水平
多色共定位同步采集
专利的光路分光与探测器同步技术,确保多色通道间无机械位移偏差,实现真纳米级共定位分析,适用于蛋白质复合体互作研究
软硬件深度集成平台
在高速共振扫描、智能曝光控制及低光毒性成像领域拥有多项实审中专利,持续推动超分辨技术从科研仪器向临床前应用延伸
