

产品概述
致微S1具备纳米级空间分辨率与多色荧光成像能力,适用于细胞生物学、神经科学、病毒学、纳米材料表征等领域,尤其擅长对亚细胞器、蛋白质复合物、纳米颗粒等超微结构进行非侵入式、高保真成像。依托中科院化学所核心研究成果,搭载自主知识产权 Stable-STED 模块,无需每日繁琐校准,即可获得高质量图像。
适用样本
兼容多种生物与材料样品,无需特殊制备流程,与现有实验工作流无缝衔接。
- 固定或活体细胞(贴壁 / 悬浮)
- 组织切片、类器官、胚胎
- 纳米材料、量子点、聚合物微球
- 病毒颗粒、外泌体、生物大分子复合物
适用领域
覆盖从基础科学研究到临床前药物开发的全链条需求。
检测原理
传统光学显微镜受限于阿贝衍射极限(~250 nm),难以分辨纳米尺度结构。STED(受激发射损耗)技术通过环形损耗光束抑制周边荧光发射,仅保留中心极小区域发光,从而将横向分辨率突破至 40 nm 以下。
致微S1 搭载自主知识产权的 Stable-STED 模块(依托中科院化学所研究成果),采用全光纤激光耦合设计确保光路长期稳定性,无需每日繁琐校准即可获得高质量图像。兼容标准荧光染料(Alexa Fluor 系列、EGFP 等),无需特殊探针,现有实验流程无需改动。
检测案例
以下案例对比展示共聚焦(Confocal)与 STED 超分辨成像的实测效果差异。
使用 Alexa Fluor 488 标记 COS-7 细胞的微管蛋白,对比共聚焦与 STED 超分辨成像效果。STED 技术可清晰分辨约 40 nm 的微管结构,突破光学衍射极限。
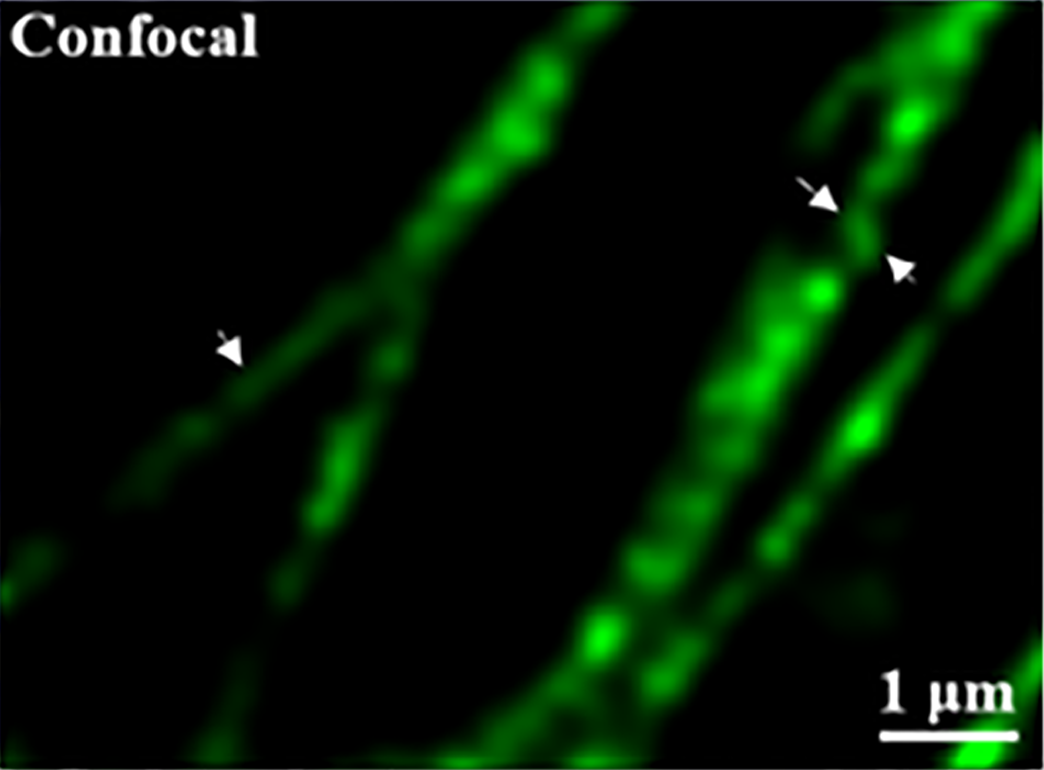
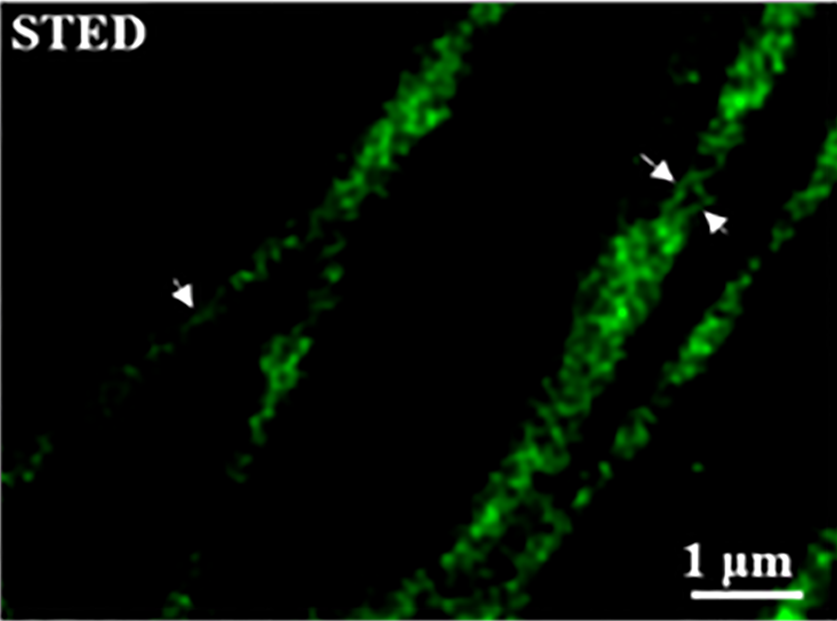
分辨率对比:~250 nm (Confocal) vs ~40 nm (STED)
肌动蛋白(Actin)是细胞骨架的重要组成部分,在细胞运动、分裂和形态维持中发挥关键作用。STED 超分辨成像可清晰显示肌动蛋白纤维的精细结构和空间分布。


清晰显示肌动蛋白应力纤维的精细结构
高尔基体是细胞内重要的膜性细胞器,负责蛋白质的加工、分选和运输。STED 超分辨技术可清晰分辨高尔基体的扁平囊泡结构和复杂的膜网络。
高尔基体扁平囊泡结构的精细呈现
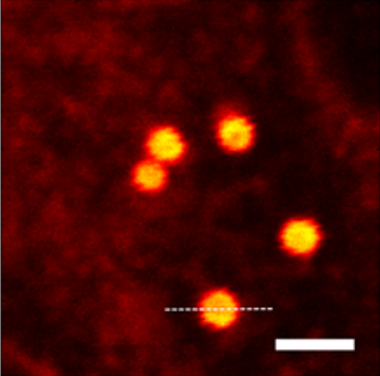
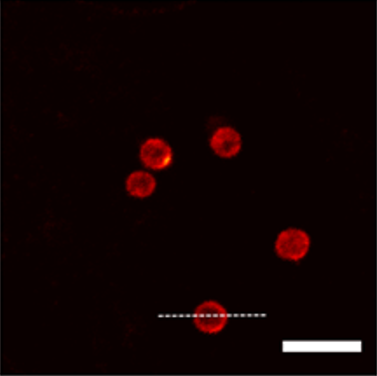
使用标准荧光微球进行系统分辨率标定,验证 STED 系统的成像性能。微球的精确尺寸和均匀荧光分布为系统校准提供了可靠的参考标准。


荧光微球直径:~100 nm,STED 下清晰可见
技术规格
| 参数 | 致微S1 |
|---|---|
| 产品型号 | 致微S1 |
| 适用样本 | 玻片、培养皿、多孔板(兼容标准载物台) |
| 激光配置 | 561 / 640 nm(激发);775 nm(STED损耗) |
| 横向分辨率 | ≤ 40 nm |
| 扫描速度 | > 1 fps @ 512×512 px(共振扫描模式) |
| 成像范围 | 100 μm × 100 μm(最大) |
| 成像模式 | 支持 x、y、z、t 多维度扫描;共聚焦 / STED 双模切换 |
| Z轴步进精度 | 1 nm |
| 物镜 | 100× 浸油物镜,NA 1.45 |
首台商业化样机 · 计划 2026 年 Q2 交付